2024.04.03
コルチゾール産⽣腫瘍の前駆病変を世界で初めて発⾒ 〜副腎腫瘍の発⽣メカニズムの解明と副腎⽪質疾患の治療への応⽤に期待〜(病態制御内科学分野 小川佳宏 主幹教授)
コルチゾール産⽣腫瘍の前駆病変を世界で初めて発⾒
〜副腎腫瘍の発⽣メカニズムの解明と副腎⽪質疾患の治療への応⽤に期待〜
〜副腎腫瘍の発⽣メカニズムの解明と副腎⽪質疾患の治療への応⽤に期待〜
ポイント
① 副腎⽪質に発⽣するコルチゾール産⽣腫瘍の前駆病変を世界で初めて発⾒
② 副腎⽪質細胞から前駆病変を経てコルチゾール産⽣腫瘍が発⽣する仕組みを解明
③ ヒト副腎⽪質の形成・維持機構の解明と副腎⽪質機能低下の治療への応⽤に期待
② 副腎⽪質細胞から前駆病変を経てコルチゾール産⽣腫瘍が発⽣する仕組みを解明
③ ヒト副腎⽪質の形成・維持機構の解明と副腎⽪質機能低下の治療への応⽤に期待
【概要】
ヒトの副腎⽪質は球状層、束状層、網状層からなる 3 層構造を形成し、3 層特異的に、⽣命維持に不可⽋なステロイドホルモン(アルドステロン、コルチゾール、副腎アンドロゲン)を分泌します。
副腎⽪質の構造は動物の種類により⼤きく異なっており、ヒトの副腎⽪質 3 層構造の形成・維持機構は、⼗分に解明されていません。副腎⽪質にはしばしばホルモンを産⽣する腫瘍が発⽣します。クッシング症候群※1 を引き起こすコルチゾール産⽣腫瘍(CPA)は、GNAS※2 や PRKACA※3 などの遺伝⼦変異を有することが報告されていますが、その発⽣機構は明らかではありませんでした。
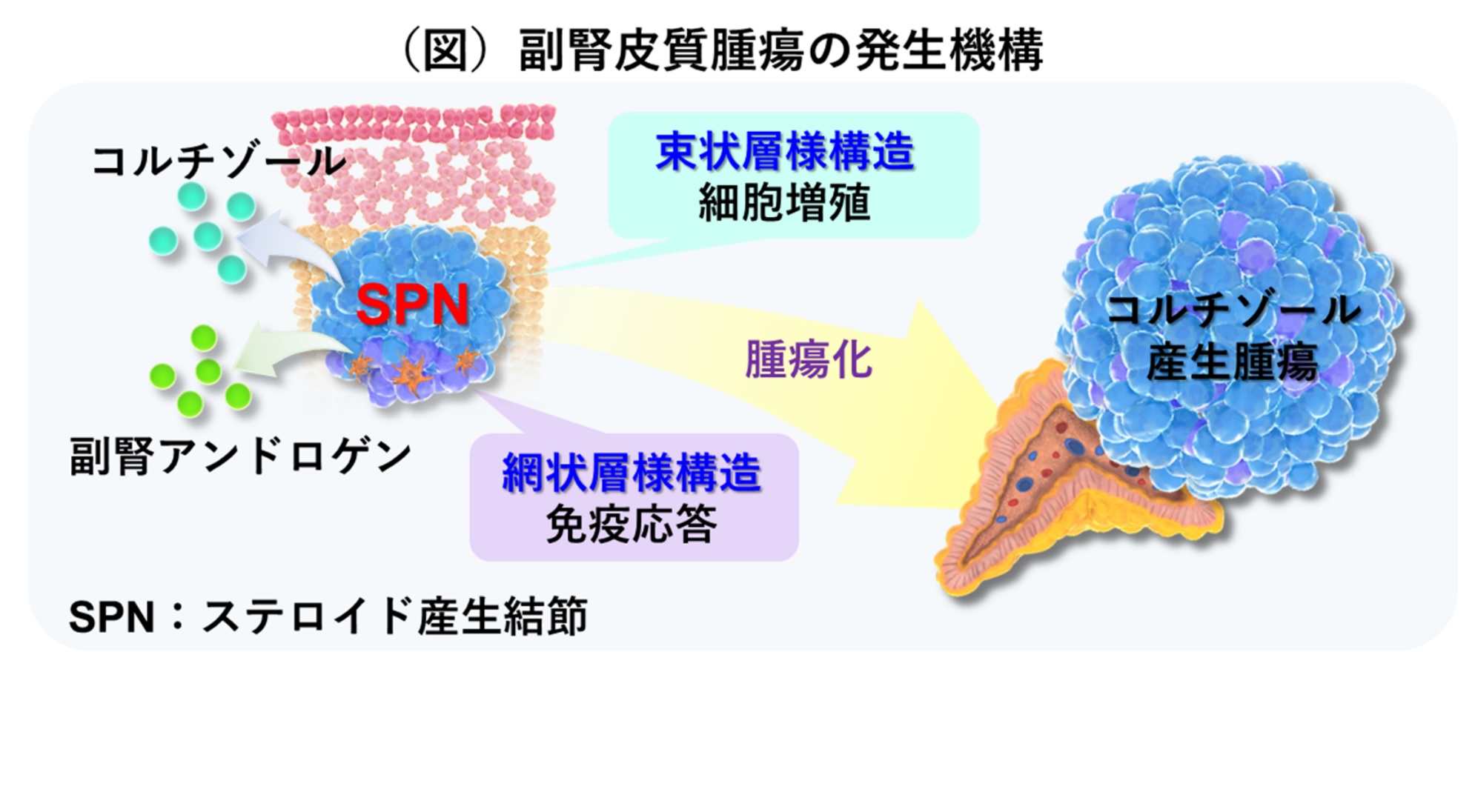
九州⼤学⼤学院医学研究院 ⼩川佳宏主幹教授と京都⼤学⼤学院医学研究科腫瘍⽣物学講座 ⼩川誠司教授を中⼼とする研究グループは、東京⼤学⼤学院新領域創成科学研究科メディカル情報⽣命専攻 鈴⽊穣教授らとの共同研究により、GNAS 変異を有する副腎⽪質内の微⼩病変として「ステロイド産⽣結節(steroids-producing nodule: SPN)」を世界で初めて発⾒しました。ゲノム解析※4や空間トランスクリプトーム解析※5 などの最新技術を駆使し、遺伝⼦変異した細胞がクローン増殖して SPN を形成し、SPN を前駆病変として CPA に進展することを明らかにしました。興味深いことに、SPN は束状層様構造と網状層様構造による特徴的な 2 層構造を呈します(図)。束状層様構造には細胞増殖を促進する作⽤、網状層様構造には免疫応答により増殖を抑制する作⽤があり、この 2 層構造が腫瘍形成において相反する効果を持つことを⽰しました。また、SPN の層構造の形成にはGNAS 変異による PKA 経路※6の亢進が関与することが明らかになりました。
本研究成果は、副腎腫瘍の発⽣機構とヒト副腎⽪質の形成・維持機構の理解に新たな知⾒をもたらすとともに、ヒトの副腎⽪質層構造の形成・維持機構の解明に向けて⼤きな⼿掛かりになり、今後、副腎腫瘍の治療や、副腎⽪質萎縮による副腎⽪質機能低下症の予防や治療への応⽤が期待されます。
本研究の成果は、英国の科学雑誌 『eBioMedicine』に、2024 年 4 ⽉ 3 ⽇(⽔)午前 0 時(⽇本時間)に掲載されました。
ヒトの副腎⽪質は球状層、束状層、網状層からなる 3 層構造を形成し、3 層特異的に、⽣命維持に不可⽋なステロイドホルモン(アルドステロン、コルチゾール、副腎アンドロゲン)を分泌します。
副腎⽪質の構造は動物の種類により⼤きく異なっており、ヒトの副腎⽪質 3 層構造の形成・維持機構は、⼗分に解明されていません。副腎⽪質にはしばしばホルモンを産⽣する腫瘍が発⽣します。クッシング症候群※1 を引き起こすコルチゾール産⽣腫瘍(CPA)は、GNAS※2 や PRKACA※3 などの遺伝⼦変異を有することが報告されていますが、その発⽣機構は明らかではありませんでした。
九州⼤学⼤学院医学研究院 ⼩川佳宏主幹教授と京都⼤学⼤学院医学研究科腫瘍⽣物学講座 ⼩川誠司教授を中⼼とする研究グループは、東京⼤学⼤学院新領域創成科学研究科メディカル情報⽣命専攻 鈴⽊穣教授らとの共同研究により、GNAS 変異を有する副腎⽪質内の微⼩病変として「ステロイド産⽣結節(steroids-producing nodule: SPN)」を世界で初めて発⾒しました。ゲノム解析※4や空間トランスクリプトーム解析※5 などの最新技術を駆使し、遺伝⼦変異した細胞がクローン増殖して SPN を形成し、SPN を前駆病変として CPA に進展することを明らかにしました。興味深いことに、SPN は束状層様構造と網状層様構造による特徴的な 2 層構造を呈します(図)。束状層様構造には細胞増殖を促進する作⽤、網状層様構造には免疫応答により増殖を抑制する作⽤があり、この 2 層構造が腫瘍形成において相反する効果を持つことを⽰しました。また、SPN の層構造の形成にはGNAS 変異による PKA 経路※6の亢進が関与することが明らかになりました。
本研究成果は、副腎腫瘍の発⽣機構とヒト副腎⽪質の形成・維持機構の理解に新たな知⾒をもたらすとともに、ヒトの副腎⽪質層構造の形成・維持機構の解明に向けて⼤きな⼿掛かりになり、今後、副腎腫瘍の治療や、副腎⽪質萎縮による副腎⽪質機能低下症の予防や治療への応⽤が期待されます。
本研究の成果は、英国の科学雑誌 『eBioMedicine』に、2024 年 4 ⽉ 3 ⽇(⽔)午前 0 時(⽇本時間)に掲載されました。
【研究の背景と経緯】
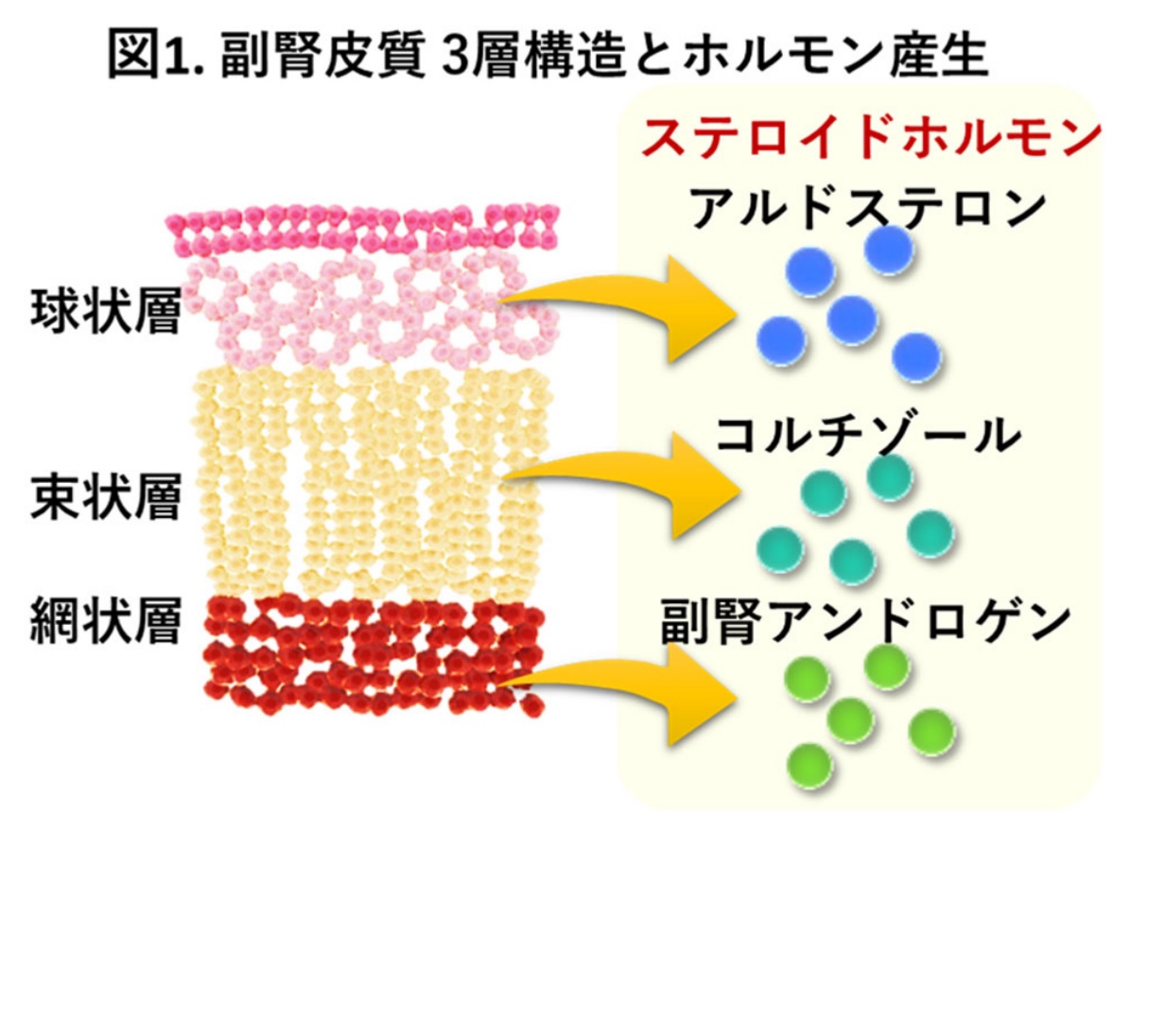
副腎⽪質は球状層、束状層、網状層の 3 層構造を形成し、3 層特異的にステロイドホルモンであるアルドステロン、コルチゾール、副腎アンドロゲンを分泌します(図1)。これらのホルモンは、⽣命の維持に重要な役割を果たしています。副腎⽪質に発⽣する腫瘍は、しばしばホルモンを過剰に産⽣します。ホルモンを産⽣する腫瘍のうち、最も頻度の⾼いコルチゾール産⽣腫瘍(CPA)はクッシング症候群の原因になります。近年、CPA の原因となる遺伝⼦変異が複数報告されましたが、CPA の発⽣機構は明らかではありませんでした。
本研究では、遺伝⼦変異を有する前駆病変が副腎⽪質内に存在すると想定し、CPA の発⽣機構を解明するために、CPA とともに⼿術で摘出された副腎⽪質を解析しました。
副腎⽪質は球状層、束状層、網状層の 3 層構造を形成し、3 層特異的にステロイドホルモンであるアルドステロン、コルチゾール、副腎アンドロゲンを分泌します(図1)。これらのホルモンは、⽣命の維持に重要な役割を果たしています。副腎⽪質に発⽣する腫瘍は、しばしばホルモンを過剰に産⽣します。ホルモンを産⽣する腫瘍のうち、最も頻度の⾼いコルチゾール産⽣腫瘍(CPA)はクッシング症候群の原因になります。近年、CPA の原因となる遺伝⼦変異が複数報告されましたが、CPA の発⽣機構は明らかではありませんでした。
本研究では、遺伝⼦変異を有する前駆病変が副腎⽪質内に存在すると想定し、CPA の発⽣機構を解明するために、CPA とともに⼿術で摘出された副腎⽪質を解析しました。
【研究の内容と成果】
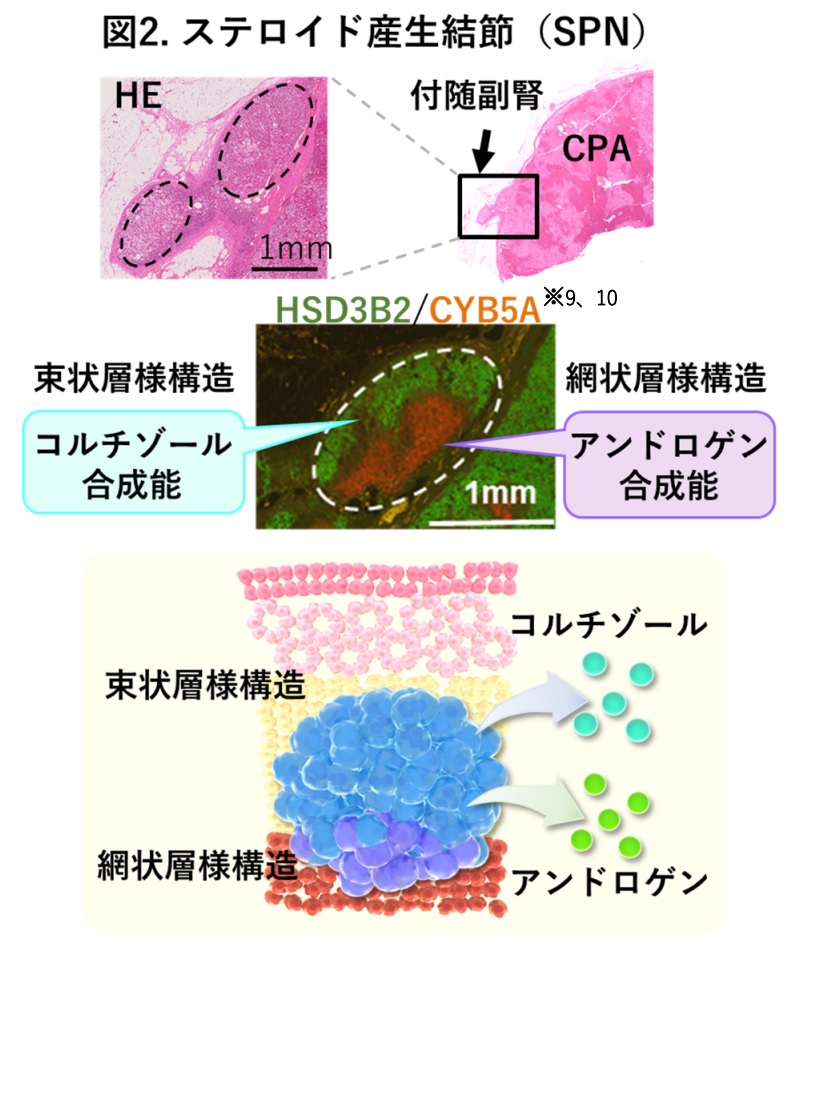
副腎⽪質の詳細な解析により、副腎⽪質内にステロイドを産⽣する微⼩病変として「ステロイド産⽣結節(steroids-producing nodule: SPN)」を世界で初めて発⾒しました(図 2)。ゲノム解析の結果、SPN において CPAの原因遺伝⼦の⼀つである GNAS 変異を同定しました。興味深いことに、SPN は束状層様構造と網状層様構造による特徴的な 2 層構造を呈していました(図 2)。RNA シーケンシング解析※7 と空間トランスクリプトーム解析により、束状層様構造は細胞増殖を促進する作⽤を持つことが明らかになりました。擬似時間解析※8から、SPN のうち束状層様構造が CPA に進展することが推定されました(図 3)。
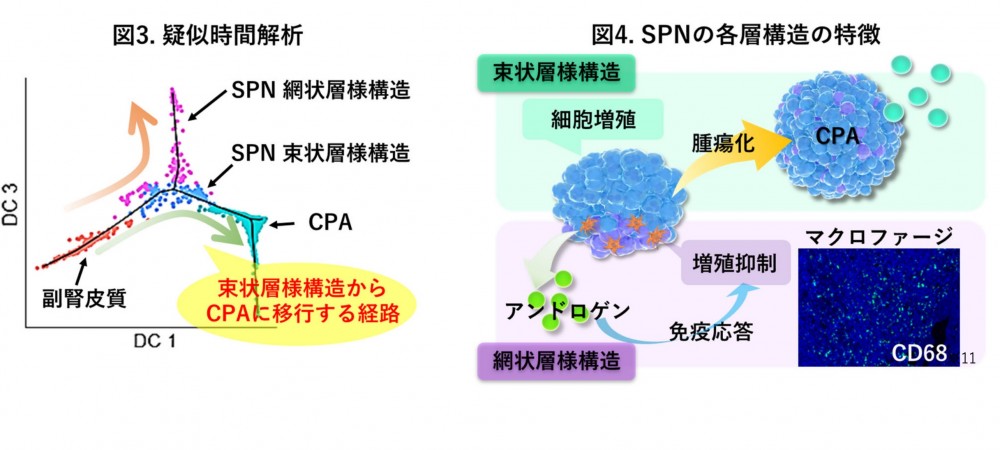
⼀⽅、網状層様構造はアンドロゲンにより誘発されるマクロファージを中⼼とした免疫応答により腫瘍の増殖を抑制する作⽤を持つことが⽰されました(図4)。これらの結果から、CPA の発⽣機構として、GNAS変異を獲得した細胞がクローン増殖して SPN を形成し、束状層様構造の増殖作⽤により SPN が CPAへと進展することが明らかになりました。
副腎⽪質の構造と機能は動物の種類により⼤きく異なります。このため、ヒトの副腎⽪質組織の形成・維持と萎縮副腎⽪質の再⽣する分⼦機構の詳細は不明です。CPA に付随する副腎⽪質は、CPA から産⽣される過剰なコルチゾールの影響で束状層と網状層が⾼度に萎縮しています。萎縮副腎⽪質内において、SPN は副腎⽪質を再⽣するかのように 2 層構造を形成します。この2層構造の形成・維持には、GNAS 変異による PKA 経路の持続的な亢進が関与することが明らかになり、副腎⽪質の束状層と網状層の形成・維持には PKA 経路が重要であることが⽰されました。
副腎⽪質の詳細な解析により、副腎⽪質内にステロイドを産⽣する微⼩病変として「ステロイド産⽣結節(steroids-producing nodule: SPN)」を世界で初めて発⾒しました(図 2)。ゲノム解析の結果、SPN において CPAの原因遺伝⼦の⼀つである GNAS 変異を同定しました。興味深いことに、SPN は束状層様構造と網状層様構造による特徴的な 2 層構造を呈していました(図 2)。RNA シーケンシング解析※7 と空間トランスクリプトーム解析により、束状層様構造は細胞増殖を促進する作⽤を持つことが明らかになりました。擬似時間解析※8から、SPN のうち束状層様構造が CPA に進展することが推定されました(図 3)。
⼀⽅、網状層様構造はアンドロゲンにより誘発されるマクロファージを中⼼とした免疫応答により腫瘍の増殖を抑制する作⽤を持つことが⽰されました(図4)。これらの結果から、CPA の発⽣機構として、GNAS変異を獲得した細胞がクローン増殖して SPN を形成し、束状層様構造の増殖作⽤により SPN が CPAへと進展することが明らかになりました。
副腎⽪質の構造と機能は動物の種類により⼤きく異なります。このため、ヒトの副腎⽪質組織の形成・維持と萎縮副腎⽪質の再⽣する分⼦機構の詳細は不明です。CPA に付随する副腎⽪質は、CPA から産⽣される過剰なコルチゾールの影響で束状層と網状層が⾼度に萎縮しています。萎縮副腎⽪質内において、SPN は副腎⽪質を再⽣するかのように 2 層構造を形成します。この2層構造の形成・維持には、GNAS 変異による PKA 経路の持続的な亢進が関与することが明らかになり、副腎⽪質の束状層と網状層の形成・維持には PKA 経路が重要であることが⽰されました。
【今後の展開】
本研究により、CPA は、前駆病変である SPN を経て発⽣することが明らかになりました。興味深いことに、SPN の2層構造は腫瘍形成において、互いに拮抗する作⽤を持つことが⽰されました(図 4)。
この研究成果は、副腎⽪質腫瘍の発⽣機構の解明と治療法の開発に新しい知⾒をもたらすものと期待されます。さらに、ヒトの副腎⽪質層構造の形成・維持機構の解明に重要な⼿掛かりを⽰しました。ステロイド製剤※12は、⾃⼰免疫性疾患(関節リウマチ、膠原病など)やアレルギー性疾患(気管⽀喘息、アトピー性⽪膚炎など)などの多くの疾患の治療薬として頻⽤される重要な薬剤です。⼀⽅、⻑期投与により副腎⽪質が萎縮し、副腎⽪質機能低下症を⽣じることが臨床的に⼤きな問題になっています。本研究成果により、今後ヒトの副腎⽪質層構造の形成・維持機構の解明が進み、副腎⽪質の萎縮による副腎⽪質機能低下症の予防や治療に応⽤されることが期待されます。
【用語解説】
(※1) クッシング症候群 体内のコルチゾールが過剰になることで、肥満や糖尿病、⾼⾎圧、⾻粗鬆症など様々な症状を引き起こす疾患です。
(※2) GNAS (GNAS 遺伝⼦) Gαs タンパク質をコードする遺伝⼦です。PKA 経路を介して、細胞内のシグナル伝達を制御し、細胞の機能や⽣理的なプロセスを調節します。
(※3) PRKACA (PRKACA 遺伝⼦) PKA の触媒サブユニットの PRKACA をコードする遺伝⼦です。
GNAS 遺伝⼦と同様に、PKA 経路を介して細胞内でのシグナル伝達や⽣理的プロセスを調節します。
(※4) ゲノム解析 ⽣物の組織から DNA を取り出し、DNA の配列を読み取ることで⽣物の遺伝⼦情報を調べる⼿法です。遺伝⼦変異などの遺伝⼦の異常を検出することができます。
(※5) 空間トランスクリプトーム解析 組織内で個々の細胞の位置情報を保持しながら⾏う RNA シーケンシング解析です。位置ごとの遺伝⼦発現を解析することができます。
(※6) PKA(cAMP 依存性タンパク質キナーゼ A)経路 細胞内のエネルギー代謝、細胞増殖、分化などのプロセスに関与する、重要な細胞内シグナル伝達経路です。副腎⽪質において、細胞内で PKA が活性化されると、ステロイドホルモンの合成が促進されます。
(※7) RNA シーケンシング解析 ⽣物の組織から RNA(DNA から遺伝情報を読み取りタンパク質の⽣成を担う分⼦)を取り出して、遺伝⼦の発現量を調べる⼿法です。どの遺伝⼦がどれだけ活発に働いているか、組織の特性などを知ることができます。
(※8) 擬似時間解析 遺伝⼦発現のパターンから擬似的な時間軸を推定し、細胞の分化を推定する解析⼿法です。
(※9) HSD3B2 ステロイド合成酵素の1つです。球状層と束状層に発現する、アルドステロンとコルチゾールの合成に必要な酵素です。
(※10) CYB5A ステロイド合成酵素の1つです。網状層に特異的に発現する、副腎アンドロゲンの合成に必要な酵素です。
(※11) CD68 マクロファージの細胞内にあるタンパク質で、マクロファージを検出するマーカーとして使⽤されます。
(※12) ステロイド製剤 体内で合成されるステロイドホルモンと似た効果を持つ薬剤です。炎症や免疫反応を抑制する作⽤があり、⾃⼰免疫性疾患やアレルギー性疾患などの多くの疾患の治療に使⽤されます。
(※1) クッシング症候群 体内のコルチゾールが過剰になることで、肥満や糖尿病、⾼⾎圧、⾻粗鬆症など様々な症状を引き起こす疾患です。
(※2) GNAS (GNAS 遺伝⼦) Gαs タンパク質をコードする遺伝⼦です。PKA 経路を介して、細胞内のシグナル伝達を制御し、細胞の機能や⽣理的なプロセスを調節します。
(※3) PRKACA (PRKACA 遺伝⼦) PKA の触媒サブユニットの PRKACA をコードする遺伝⼦です。
GNAS 遺伝⼦と同様に、PKA 経路を介して細胞内でのシグナル伝達や⽣理的プロセスを調節します。
(※4) ゲノム解析 ⽣物の組織から DNA を取り出し、DNA の配列を読み取ることで⽣物の遺伝⼦情報を調べる⼿法です。遺伝⼦変異などの遺伝⼦の異常を検出することができます。
(※5) 空間トランスクリプトーム解析 組織内で個々の細胞の位置情報を保持しながら⾏う RNA シーケンシング解析です。位置ごとの遺伝⼦発現を解析することができます。
(※6) PKA(cAMP 依存性タンパク質キナーゼ A)経路 細胞内のエネルギー代謝、細胞増殖、分化などのプロセスに関与する、重要な細胞内シグナル伝達経路です。副腎⽪質において、細胞内で PKA が活性化されると、ステロイドホルモンの合成が促進されます。
(※7) RNA シーケンシング解析 ⽣物の組織から RNA(DNA から遺伝情報を読み取りタンパク質の⽣成を担う分⼦)を取り出して、遺伝⼦の発現量を調べる⼿法です。どの遺伝⼦がどれだけ活発に働いているか、組織の特性などを知ることができます。
(※8) 擬似時間解析 遺伝⼦発現のパターンから擬似的な時間軸を推定し、細胞の分化を推定する解析⼿法です。
(※9) HSD3B2 ステロイド合成酵素の1つです。球状層と束状層に発現する、アルドステロンとコルチゾールの合成に必要な酵素です。
(※10) CYB5A ステロイド合成酵素の1つです。網状層に特異的に発現する、副腎アンドロゲンの合成に必要な酵素です。
(※11) CD68 マクロファージの細胞内にあるタンパク質で、マクロファージを検出するマーカーとして使⽤されます。
(※12) ステロイド製剤 体内で合成されるステロイドホルモンと似た効果を持つ薬剤です。炎症や免疫反応を抑制する作⽤があり、⾃⼰免疫性疾患やアレルギー性疾患などの多くの疾患の治療に使⽤されます。
【謝辞】
本研究は、JSPS 科研費 (JP22H04993, JP22K08627)、上原記念⽣命科学財団、⼤和証券財団、⾙原守⼀医学振興財団、セコム科学技術振興財団、⼩野医学研究財団、⽇本応⽤酵素協会の助成を受けたものです。
本研究は、JSPS 科研費 (JP22H04993, JP22K08627)、上原記念⽣命科学財団、⼤和証券財団、⾙原守⼀医学振興財団、セコム科学技術振興財団、⼩野医学研究財団、⽇本応⽤酵素協会の助成を受けたものです。
【論⽂情報】
掲載誌:eBioMedicine
タイトル:Steroids-producing nodules: a two-layered adrenocortical nodular structure as a precursor
lesion of cortisol-producing adenoma
著 者 名 : Tazuru Fukumoto, Hironobu Umakoshi, Norifusa Iwahashi, Tatsuki Ogasawara, Maki
Yokomoto-Umakoshi, Hiroki Kaneko, Masamichi Fujita, Naohiro Uchida, Hiroshi Nakao, Namiko
Kawamura, Yayoi Matsuda, Ryuichi Sakamoto, Takashi Miyazawa, Masahide Seki, Masatoshi Eto,
Yoshinao Oda, Yutaka Suzuki, Seishi Ogawa, and Yoshihiro Ogawa
D O I :10.1016/j.ebiom.2024.105087
掲載誌:eBioMedicine
タイトル:Steroids-producing nodules: a two-layered adrenocortical nodular structure as a precursor
lesion of cortisol-producing adenoma
著 者 名 : Tazuru Fukumoto, Hironobu Umakoshi, Norifusa Iwahashi, Tatsuki Ogasawara, Maki
Yokomoto-Umakoshi, Hiroki Kaneko, Masamichi Fujita, Naohiro Uchida, Hiroshi Nakao, Namiko
Kawamura, Yayoi Matsuda, Ryuichi Sakamoto, Takashi Miyazawa, Masahide Seki, Masatoshi Eto,
Yoshinao Oda, Yutaka Suzuki, Seishi Ogawa, and Yoshihiro Ogawa
D O I :10.1016/j.ebiom.2024.105087
【お問合わせ先】
九州⼤学⼤学院医学研究院 病態制御内科学分野 主幹教授 ⼩川 佳宏(オガワ ヨシヒロ)
TEL:092-642-5275 FAX:092-642-5297
Mail:ogawa.yoshihiro.828(a)m.kyushu-u.ac.jp
※(a)を@に置き換えてメールを送信してください
九州⼤学⼤学院医学研究院 病態制御内科学分野 主幹教授 ⼩川 佳宏(オガワ ヨシヒロ)
TEL:092-642-5275 FAX:092-642-5297
Mail:ogawa.yoshihiro.828(a)m.kyushu-u.ac.jp
※(a)を@に置き換えてメールを送信してください

