2019.10.08
老化に起因した発がんメカニズムの一部解明 がん発生予防の可能性を示唆(中津可道准教授 續輝久名誉教授)
老化に起因した発がんメカニズムの一部解明 がん発生予防の可能性を示唆
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区) 研究所 発がん・予防研究分野らの研究チームは、細胞の老化が発がんのリスク要因となるメカニズムの一部を解明することに成功しました。
がんの発生要因には、生活習慣によるもの(喫煙や飲酒、食物・栄養など)と、そうでないものが挙げられ、生活習慣によるものはこれを改善することでリスクを抑制することができます。一方、生活習慣によらないものは、リスク要因が明確ではなく、さらにがんを発生させる遺伝子の変異も無秩序に入るため、予防できないと考えられていました。
しかし、研究所 発がん・予防研究分野の研究チームは、多くの変異は無秩序に入るのではなく、細胞の老化によりDNA修復能が低下し、DNAの損傷が蓄積することで変異のリスクが上がり、がんを発生させることを見出しました。これまでの研究において、老化と発がんの関係を明確に示したものはなく、本研究によりその関係が明確になりました。
これにより、これまで予防することが出来ないと考えられていたがんについて、損傷したDNAの修復を促すなどの方法で予防できる可能性が示唆されました。
本研究は、研究所 発がん・予防研究分野 主任研究員 吉岡研一(責任著者)らの研究成果で、英国のオンライン科学雑誌「Nature communications」(9月2日付け:日本時間9月2日)に掲載されました。
【背景】
がんは、遺伝子の変異に起因して誘発されますが、ほとんどの変異は無秩序であるため、生活習慣の改善や慢性炎症の低減以外に、有効な発がん予防法の開発は困難と予想されていました。
発がん研究の分野でも、遺伝子の変異の入り方と発がんの関係には未解決の疑問が残っており、世界的にも論争が続いています。本研究は、がん抑制遺伝子への変異の入り方と、その要因が老化に起因することを明らかにしたもので、新たな予防標的が明確になりました。
【研究成果概要】
これまで、ほとんどの変異はDNA複製過程で無秩序に誘導されると考えられてきました。また、発がん過程は、がん抑制遺伝子が機能を欠損し、増殖抑制が効かなくなった細胞の出現・増殖を数回経て進行する(クローン進化*1)と考えられています。しかし、これらの誘導機構・過程には未だに不明な点が多くあります。
研究チームは、細胞の老化過程で蓄積したDNA損傷を引き金として、変異のリスクが上がるゲノム不安定性*2の状態になり、またこれに伴う変異導入に起因して、がん抑制遺伝子の変異したクローン進化が誘導されることをin vitroのモデル解析系を用いて示すことに成功しました。
DNA複製エラーは、一定頻度で無秩序に生じますが、これらはミスマッチ修復機構によって修復されます。このため、ミスマッチ修復欠損細胞では、DNA複製エラーが高頻度で誘導・蓄積することが知られています。しかし今回の研究で、がん抑制遺伝子のクローン進化は、ミスマッチ修復欠損よりゲノム不安定性により誘導され、ゲノム安定性が保持された背景では抑制されていることが分かりました。
また、ゲノム不安定性は、染色体不安定性(CIN)とマイクロサテライト*3不安定性(MSI)のふたつに大別されますが、本研究において両者は相互排他的であることが示され、中高年以降に発症したがんではどちらか一方が認められることを裏付けました。また、マイクロサテライト不安定性の誘導機構も明らかになり、新たな研究展開が期待されます。
図A
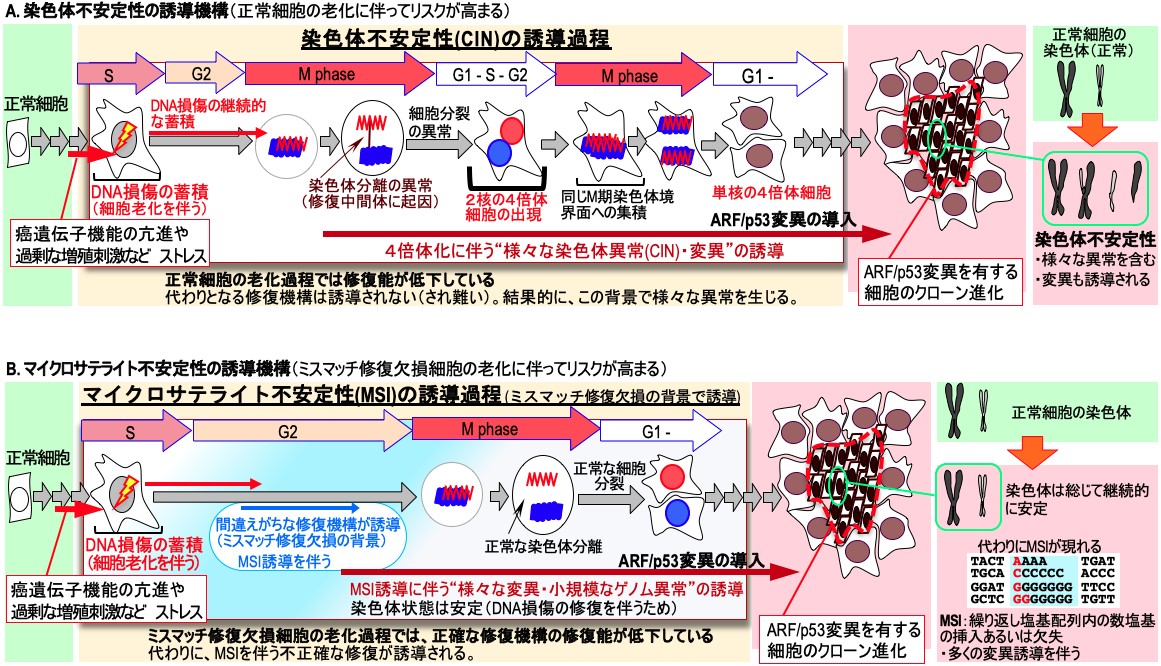
染色体不安定性の誘導機構(正常細胞の老化に伴ってリスクが高まる)
染色体不安定性(CIN)は、老化した細胞背景(DNA損傷修復能の低下した状態)で、DNAの複製過程で生じた損傷に起因して誘導される。この損傷が、修復されずに持続的に蓄積するが、結果的に様々な異常な染色体が生じる。変異の誘導を伴う。
図B
マイクロサテライト不安定性の誘導機構(ミスマッチ修復欠損細胞の老化に伴ってリスクが高まる)
マイクロサテライト不安定性(MSI)は、ミスマッチ修復欠損細胞が老化した背景で、DNAの複製過程で生じた損傷に起因して誘導される。老化に伴って“正確な修復機構の修復能が低下”するが、代わりに“間違えがちな修復機構”が誘導され、マイクロサテライト不安定性はこの“間違えがちな修復”に伴って生じる。この背景では、多くの変異誘導を伴うが、DNA損傷は修復されるため、染色体不安定性は抑制される。
【展望】
本研究で、老化に起因するがんは、ゲノム不安定性を伴い変異導入されることが示されたことから、今後、研究チームは、損傷したDNAの修復によるゲノム安定性の保持について研究を進め、新たながん予防応用へ研究を展開します。
また、ゲノム不安定性のリスク要因、ゲノム不安定性リスクの上昇要因への研究展開も期待され、その解析からは、外的なリスク要因等(放射線や紫外線などを含む)による発がんへの影響とそのリスク要因が明確になることも期待されます。
【発表論文】
雑誌名: Nature communications
タイトル: Replication stress triggers microsatellite destabilization and hypermutation leading to clonal expansion in vitro
著者:国立がん研究センター
研究所 任意研修生 松野悠介 (筆頭著者)、熱海悠子、清水敦拡、藤森遥、兵頭舞、皆川祐輔
研究所 主任研究員 吉岡研一 (責任著者)
研究所 ユニット長 金子修三
研究所 分野長、理化学研究所 革新知能統合研究センター チームリーダー 浜本隆二
東京大学
医科学研究所 助教 片山琴絵
医科学研究所 教授 宮野悟
名古屋大学
医学系研究科 教授 島村徹平
九州大学
医学研究院 准教授 中津可道
医学研究院 名誉教授 續輝久
国立遺伝学研究所
所長、学習院大学理学部 客員研究員 花岡文雄
DOI: 10.1038/s41467-019-11760-2
URL: https://www.nature.com/articles/s41467-019-11760-2
【用語解説】
*1 クローン進化:
がん細胞に遺伝子変異が無秩序に生じて生成されたサブクローンが自然淘汰され環境に適合するように進化すること。
*2ゲノム不安定性:
ゲノムが損傷を受けると修復機構により修復されますが、修復に失敗した場合には遺伝子異常が蓄積します。修復機能が低下した状態では細胞分裂の際に正しいコピーを生成することができずに、様々な遺伝子を持った細胞が生成されるようになります。このような状態がゲノム不安定性と呼ばれます。
*3 マイクロサテライト:
ゲノム上に存在する塩基配列の単純な繰り返しからなるもので、DNA鑑定などに利用されている。
【問い合わせ先】
医学研究院 基礎放射線医学分野 准教授 中津 可道
nakatsu★biophys.med.kyushu-u.ac.jp(★を@に書き換えてください)

