2024.09.26
上皮細胞シートに生じた欠損を速やかに修復する仕組みの解明 ~アトピー性皮膚炎や炎症性腸疾患など上皮バリアの異常による病態の理解に繋がる知見~(生化学分野 池ノ内 順一教授)
ポイント
- 体の表面を構成する上皮細胞シートのバリアが破綻すると炎症性疾患の原因になります。
- 上皮細胞シートの中でダメージを受けた細胞を、周りの細胞が迅速に排除することで、上皮細胞のバリアを安定に維持する仕組みを明らかにしました。
- 上皮細胞シートのバリア機能が低下することで起こるアトピー性皮膚炎や炎症性腸疾患などの病態解明や予防法の開発に役立つ知見です。
概要
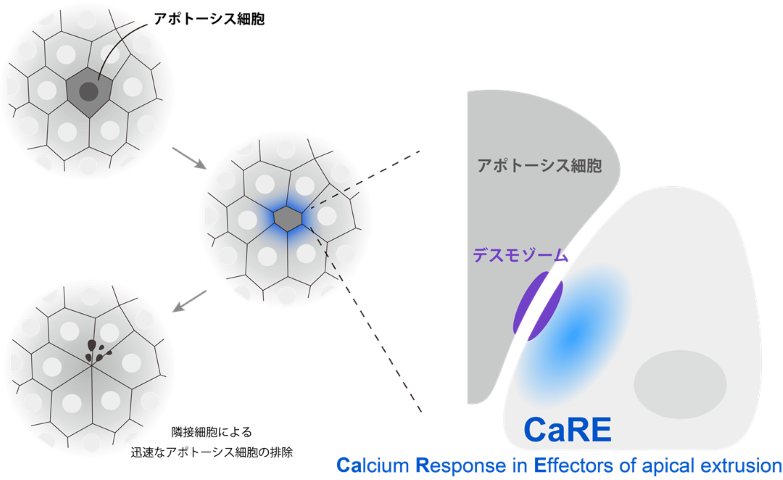
私たちの体は上皮細胞のシートによって、外界からの異物の侵入を防いでいます。体の表面に位置する上皮細胞は、常に様々なストレスに曝されており、ダメージを受けた細胞はアポトーシス(細胞死)*1を起こします。アポトーシスを起こした細胞が、上皮細胞シート内に残り続けると、細胞シートの欠損部位となり、そこから異物の侵入が起こり、感染や炎症の原因になります。このため、アポトーシスを起こした細胞は、周囲の細胞によって迅速に細胞シートから排除する必要がありますが、どのように周囲の細胞がアポトーシスを起こした細胞を排除するかは詳しく明らかになっていませんでした。
今回の研究では、アポトーシス細胞に隣接した細胞において、アポトーシス細胞と接着した領域でカルシウムイオンが持続的に上昇する現象(CaRE と命名)を見出し、この現象がアポトーシス細胞の効率的な排除に不可欠であることを明らかにしました。
九州大学大学院医学研究院の池ノ内順一教授、システム生命学府一貫制博士課程5年の長佑磨は、上皮細胞同士の機械的な連結にのみ関わっていると考えられてきたデスモゾーム*2と呼ばれる細胞接着装置に、細胞内カルシウムイオン動態の制御に関わる小胞体 IP3 受容体が集積していることを見出しました。また、アポトーシス細胞と隣接細胞の接着面において、デスモゾームを介したカルシウムイオンの持続的上昇 (CaRE) とそれによる接着面の収縮がアポトーシス細胞の排除に必須であることを見出しました。
本研究によって得られた知見は、アトピー性皮膚炎や炎症性腸疾患などの上皮バリアの破綻による病態の解明や慢性炎症の新たな予防法や治療法の開発に資する知見です。本研究成果は、英国の科学雑誌 Current Biology に2024年9月23日(日本時間)に掲載されました。
研究者からひとこと
皮膚を引っ張っても千切れないように、上皮細胞はデスモゾームなどの細胞接着装置を介して機械的に結合し、シートを形成しています。デスモゾームは細胞同士を強固に糊づけする役割のみが想定されていましたが、予想外なことに細胞内のカルシウムイオンを介してアポトーシス細胞の排除に関わることが明らかになりました。
研究の背景と経緯
私たちの体の表面(皮膚)や消化管の表面は、上皮細胞のシートによって覆われており、外界からの異物の侵入を防ぐバリアとして機能しています。上皮細胞シートは外界に常に面していることから、摩擦などの機械的なストレスや紫外線ストレスなど様々なストレスに曝されており、ダメージを受けた細胞は細胞死(アポトーシス)を起こし、絶えず細胞がリニューアルされています。アポトーシスを起こした細胞(以下、アポトーシス細胞)が、上皮細胞シートに残存すると、細胞シートの欠損部位となり、そこから、様々な異物が体内に侵入することを許してしまいます。上皮細胞シートのバリアの破綻は、アトピー性皮膚炎や炎症性腸疾患の原因となるため、上皮細胞シート内に生じたアポトーシス細胞は、迅速に除去する必要があります。
これまでに、アポトーシス細胞が生じると、隣接した上皮細胞が積極的にその細胞を排除することが知られていました (Rosenblatt et al. 2001; Takeuchi et al. 2020)。また、その際に、デスモゾームと呼ばれる接着構造が重要であることも報告されていました (Thomas et al. 2020)。しかしながら、アポトーシス細胞の排除において、デスモゾームがどのような役割を果たしているかについては、不明のままでした。
研究の内容と成果
九州大学システム生命学府一貫制博士課程5年の長佑磨、理学研究院の松沢健司講師、医学研究院の池ノ内順一教授、および東京大学大学院医学系研究科の本田郁子准教授、北海道医療大学の谷村明彦教授から成る研究グループは、本研究において、上皮細胞シートにおいてアポトーシス細胞の迅速な排除に関わる新しい分子機構を見出しました。
今回、研究グループは、細胞内カルシウムイオンの濃度変化を検出するプローブ (GCaMP6) を形質膜に標的化させた細胞を用いることで、アポトーシス細胞の排除の際に起こるカルシウムイオンの動態を詳細に解析しました。その結果、アポトーシス細胞に隣接した細胞内のアポトーシス細胞との接着面において、持続的にカルシウムイオンの上昇が認められることを見出し、この現象を、Calcium Response in Effectors of apical extrusion (CaRE) と名付けました。
CaRE は、接着面に限局して観察されることから、細胞接着装置が関与するのではないかという仮説を立てて解析を進めた結果、デスモゾームと呼ばれる細胞接着装置に、カルシウムイオンの制御に関わる小胞体の IP3 受容体が近接していることを見出しました。アポトーシス細胞に隣接した上皮細胞では、デスモゾームの近傍で IP3 受容体の活性化が起こることで、細胞接着領域のカルシウムイオンが持続的に上昇し、それによって細胞接着構造を裏打ちするアクトミオシン線維の収縮が促進されます。アポトーシス細胞に接している隣接細胞の接着面がアクトミオシン線維によって収縮することにより、アポトーシス細胞をシートから絞り出して排除することを明らかにしました。
今後の展開
研究グループは、CaRE に関与する分子として、デスモゾームの構成因子、 IP3 受容体、およびデスモゾームと IP3 受容体を連結する分子である K-Ras 誘導アクチン結合タンパク質 (KRAP) を同定しました。今後は、CaRE に関与する因子のさらなる探索に加え、デスモゾーム近傍に位置する IP3 受容体を介したカルシウムイオンの制御機構が、どのような生理的意義を持つか、または病態発症においてどのような役割を果たしているかについて、さらなる解明を進めていきます。
参考図
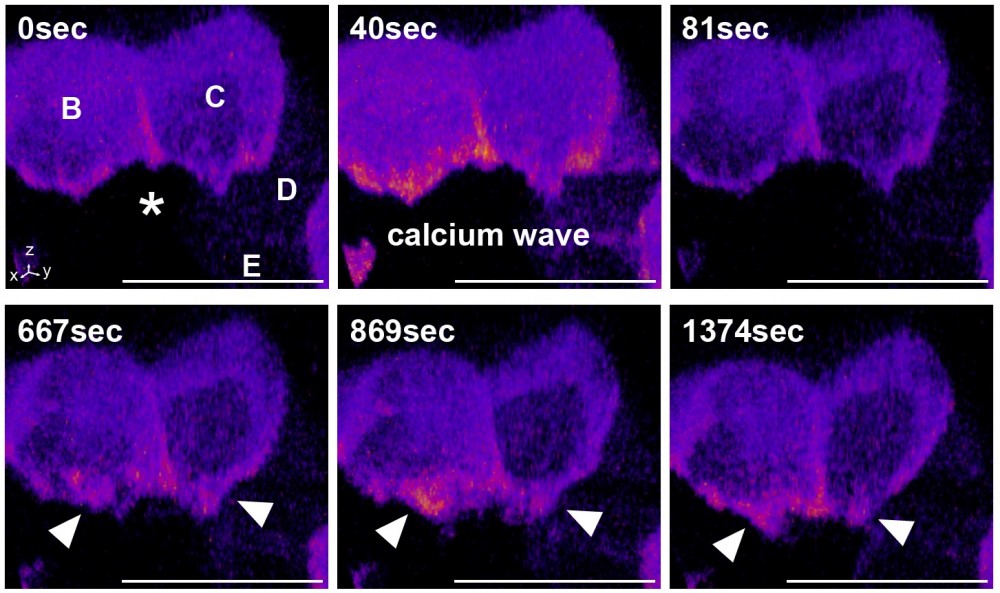
図1 アポトーシス細胞に隣接した上皮細胞に認められる持続的なカルシウムイオンの上昇
カルシウムイオンに対するプローブである GCaMP6 を形質膜に標的化させることにより、形質膜におけるカルシウムイオン動態を詳細に解析した結果、アポトーシス細胞と接着している細胞では、その接着面において持続的なカルシウムイオンの上昇(矢頭)が認められることが明らかになりました。
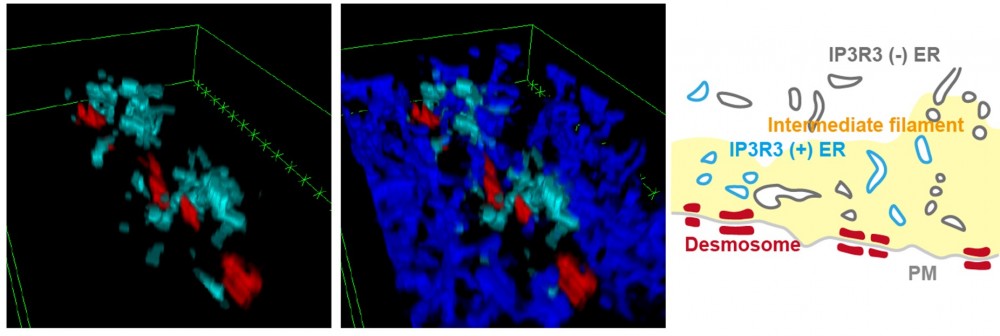
図2 光-電子相関顕微鏡法(CLEM)によるIP3受容体の局在の解析
デスモゾーム(赤色)の近傍に、小胞体(青色)の中でも特に、IP3 受容体(水色)を含む小胞体の一部が集積していることを見出しました。
用語解説
- *1 アポトーシス
- 紫外線による DNA 損傷などで不可逆的なダメージを受けた細胞は、個体の健全さを保つために、能動的に細胞死を引き起こします。この細胞死の形式をアポトーシスと呼びます。
- *2 デスモゾーム
- 細胞同士が接着してシートを形成する上皮細胞には、機能や形態が異なる複数の細胞接着装置が存在します。デスモゾームは、皮膚や心筋など、機械的な負荷を受ける細胞で多く見られる細胞接着構造です。
謝辞
本研究は、文部科学省 日本学術振興会 科学研究費 (JP22H02618, JP23K18141, JP23KJ1689, JP22K06225)、科学技術振興機構 創発的研究若手挑戦事業 (JPMJFR204L)、ERATO (JPMJER1702) 等の支援を受けて行われました。
論文情報
- 掲載誌:
- Current Biology
- タイトル:
- A sustained calcium response mediated by IP3 receptor anchoring to the desmosome is essential for apoptotic cell elimination
- 著者名:
- Yuma Cho, Ikuko Koyama-Honda, Akihiko Tanimura, Kenji Matsuzawa and Junichi Ikenouchi
- DOI:
- 10.1016/j.cub.2024.08.057
お問合せ先
九州大学 大学院医学研究院 生化学分野
教授 池ノ内 順一(いけのうち じゅんいち)
092-802-4292 092-802-4292 ikenouchi.junichi.033(at)m.kyushu-u.ac.jp

