2026.03.12
生きたまま組織を透明化できる試薬の開発 ~正常機能を保持したまま透明化して神経細胞の活動を蛍光観察することに成功~(疾患情報研究分野 今井 猛教授、稲垣 成矩助教)
- 血液中に多く含まれるタンパク質、アルブミン*1を用いることで、哺乳類の生きた組織の透明化を実現しました。
- 細胞外液のイオン組成をほとんど変えることなく、神経細胞の正常な機能を維持したまま、脳組織を透明化することができました。
- 生きた動物の脳組織において、従来よりも深部まで蛍光顕微鏡観察が可能になりました。
哺乳類の生体組織の多くは不透明であり、光を使って組織の深部を観察することは困難です。死後にホルマリンなどで固定した組織標本については、近年、透明化試薬を使って透明化し、深部まで観察することが容易になりました。しかし、従来の透明化試薬は毒性や浸透圧*2が高く、細胞機能を維持することは困難でした。そのため、生きた哺乳類組織の透明化は実現していませんでした。
本研究では、細胞の正常な機能を維持したまま、生きた組織の深部観察を可能にする透明化試薬「SeeDB-Live」を開発しました (図1)。九州大学大学院医学研究院の今井猛主幹教授、稲垣成矩助教、鹿児島大学、山梨大学らの研究グループは、生きた組織が不透明に見える主な原因が、細胞の内外で光が屈折*3・散乱*4し、まっすぐ進まないためであることを見出しました。そこで、細胞外液にタンパク質の一種であるアルブミンを加え、光の屈折・散乱を抑えることで、生きた組織を非侵襲的に透明化できることを示しました。アルブミンは、細胞外液のイオン組成をほとんど変えず、細胞毒性もありません。そのため、生体組織を透明化した状態で、組織中の細胞の正常な機能を蛍光顕微鏡観察することが初めて可能となりました。
アルブミンを用いた透明化試薬 SeeDB-Live により、取り出した脳組織や生きたマウスの脳を非侵襲的に透明化し、組織深部における微細構造や神経活動の観察が可能になりました。本成果は、これまで困難だった組織深部における生体機能の計測を可能にし、神経科学や発生生物学など広く生命科学分野の発展に寄与することが期待されます。
本研究成果は、2026年3月12日 (木) 午後7時に米国の科学雑誌 Nature Methods に掲載されました。

図1 生きた脳組織の透過画像と二光子励起顕微鏡画像
研究者からひとこと
今回、生きた細胞の光学的特性を緻密に調べたことと、分子量が大きな分子に着目したことが鍵となり、世界で初めて生きた組織の非侵襲的な透明化を実現しました。ありふれたタンパク質を培地に加えるだけで、組織の正常な機能を維持したまま透明化できることは驚きでした。アルブミンは元々血液中に高濃度に含まれているだけあり、タンパク質の中でもとりわけ溶解度が高く、透明化には最適でした。(稲垣・今井)
近年、細胞内の様々な分子の機能を観察できる蛍光センサー*5の開発が進み、生きた細胞内の分子の挙動を、リアルタイムに観察できるようになりました。しかし、生体組織には、細胞をはじめ、様々な構造が詰め込まれており、それらの境界では光が複雑に屈折・散乱します。このため、生体組織は一般的に不透明であり、深部に位置する細胞を光で観察することは困難でした。深部観察に適した二光子励起顕微鏡*6を使っても、観察できるのは深さ数百マイクロメートル (1マイクロメートルは1000分の1ミリメートル) までが限界でした。
死後にホルマリンなどで固定した組織標本であれば、近年、透明化試薬 (例えば SeeDB や SeeDB2 など) を使って透明化することが可能となり、深部観察が容易になりました。これらの方法では、透明化試薬を組織に浸透させて、組織内の屈折率*7を均一化します。その結果、屈折・散乱が抑えられて組織が透明になり、深部を含む組織全体を見通す蛍光観察が可能となりました。しかし、こうした従来の透明化試薬は毒性が高いうえ、浸透圧が極めて高く、細胞の正常な機能を保持できませんでした。そのため、生きた哺乳類組織の透明化は実現していませんでした。
生きた生体組織を、機能を損なうことなく透明化し、深部の観察を実現することは、生命科学分野における長年の課題であり、多くの研究者の夢でもありました。
生きた組織の透明化を実現するには、組織中の屈折率を均一化して透明にするだけでは不十分です。細胞に対する毒性を抑えるとともに、細胞外液の浸透圧やイオン組成などを生きた組織に極力近づけ、細胞機能を正常に保つことが重要です。これまで、これらの条件を全て満たす「生きた組織の透明化試薬」は実現していませんでした。
研究グループは、生きた細胞を透明にするために、まず最適な細胞外液の屈折率を調べました。生きた培養細胞を様々な屈折率の液体に浸して光の透過しやすさを検討した結果、細胞外液の屈折率を1.36-1.37にすると生きた細胞が最も透明になることを見出しました (図2A)。通常の細胞外液の屈折率が1.33-1.34であるのに対して、細胞内の屈折率は1.36-1.37です。そのため、通常の培地中では、光が細胞に当たると、屈折・散乱してしまいます。研究グループは、生きた細胞が透明になったのは、細胞外液の屈折率が細胞内と一致したことにより、光の屈折・散乱が抑えられたからだと考えました (図2B)。これは、ビー玉を屈折率の同じ液体に浸すと、光の屈折・散乱が抑えられて透明に見えるのと同じ原理です (図2C-E、動画1)。また、予想外なことに、生きた細胞が透明になる条件は、従来、固定した死細胞を透明化するのに用いられていた屈折率条件 (屈折率1.43-1.56) とは大きく異なっていました。
研究グループは次に、生体の浸透圧に近い条件で細胞外液の屈折率を1.36-1.37に合わせる方法を検討しました。従来の透明化試薬では、屈折率を1.36-1.37に上げようとすると、浸透圧が通常の細胞外液の数倍にもなってしまうため、細胞機能が損なわれてしまいます。細胞膜は半透膜 (水は通しやすいが溶質やイオンは通しにくい) であり、細胞質中の水分が浸透圧の高い細胞外へと流出してしまうためです (図3A)。浸透圧は、溶液の単位体積あたりに含まれる分子の数が多いほど大きくなることが知られています。そこで、研究グループは、分子量の小さな分子を多数使う代わりに、分子量の大きな分子 (高分子量分子) を少数使って屈折率を上げれば、浸透圧の上昇を抑えられるだろうと考えました (図3B)。様々な高分子量分子について、屈折率が1.365となる条件で浸透圧を計測したところ、血液中に含まれるタンパク質の一種であるアルブミンの水溶液が最も低い浸透圧を示すことが分かりました。細胞外液のイオン組成を保持したまま屈折率が1.365になるようにアルブミンを加えても、浸透圧の上昇はごくわずかでした (一般的な細胞外液の浸透圧が約280 mOsm/kg であるのに対して、アルブミンによる浸透圧上昇は約3 mOsm/kg)。
実際に、アルブミンを溶かして屈折率を調整した培地中でも、培養細胞が3日間にわたって正常に増殖することを確認しました (図4A)。このことから、細胞に対する毒性が限りなく低いことが分かりました。研究グループは、この透明化培地を「SeeDB-Live」と名付けました。
培養細胞を立体的に培養して作製したスフェロイド (細胞塊)*8を、SeeDB-Live に浸すと、15分ほどで透明になることが確認されました (図4B、C、動画2)。透明化後には、蛍光タンパク質を発現する細胞を、透明化前と比べて2倍ほどの深さまで観察できました (動画3)。腸の上皮細胞を試験管内で培養した腸オルガノイド*9についても、SeeDB-Live で透明化して観察できました (図4B)。
次に、マウスから取り出したばかりの脳組織も、SeeDB-Live に浸すと1時間ほどで透明になることが確認されました (図5A、動画4)。電気生理学的な計測を行ったところ、神経細胞の膜電位の特性や活動動態はほとんど損なわれないことが分かりました。また、蛍光カルシウムセンサー GCaMP を用いたカルシウムシグナルの計測により、透明化前と同様の正常な発火 (神経の電気的な活動) が、透明化後にも維持されていることが確認されました。さらに、通常では計測が難しい組織深部においても、神経細胞のカルシウムシグナルを計測することができました (図5B、動画5)。
続いて、生きたマウスの脳を対象として、SeeDB-Live による透明化を試みました。SeeDB-Live を1時間ほどかけて脳表面から浸透させたところ、脳深部に位置する神経細胞の蛍光を、透明化前と比べて3倍以上明るく観察できました (図6A、B、動画6、動画7)。その結果、通常では難しかった大脳皮質の深部 (深さ約500マイクロメートルの第5層) における神経細胞の微細構造も明瞭に観察することができました (図6C、D)。さらに、GCaMP を用いることで、大脳皮質の深部における神経細胞のカルシウムシグナルも、高い精度で計測することができました (図7)。
SeeDB-Live で生きた組織を透明化する際には、細胞外液を一時的に SeeDB-Live に置換します。そのため、生きた動物の脳の場合、透明化処理の後、数時間で SeeDB-Live は洗い流されて、透明度は元の状態に戻ります。長期間にわたって同じ動物で蛍光観察するには、その都度、SeeDB-Live を脳に浸透させ、透明化する必要がありました。私たちは、生きたマウス脳の透明化を4ヶ月以上にわたって繰り返し行い、神経細胞のカルシウムシグナルを計測できることを示しました。その際、マウス脳内の炎症や行動異常も見られなかったことから、SeeDB-Live による透明化処理は脳の正常な機能を損なわないことが分かりました。
本研究で開発された SeeDB-Live を用いることで、生きた組織の深部における蛍光観察を利用した研究が加速すると期待されます。特に、これまで困難であった脳深部の観察が可能となり、脳機能の理解がさらに進むと考えられます。将来的には、マウスだけでなく、より深部の観察が難しい霊長類の脳機能計測にも応用できる可能性があります。また、オルガノイドのようなミニ臓器においても、組織深部を観察できるようになり、薬剤開発のための機能的スクリーニングに活用されることが期待されます。本研究は、生きたままの透明化を実現した重要な第一歩ですが、今後は、生きた組織中に SeeDB-Live を効率良く導入するための手法を開発することで、さらに透明化の適用範囲や用途を広げることが課題です。
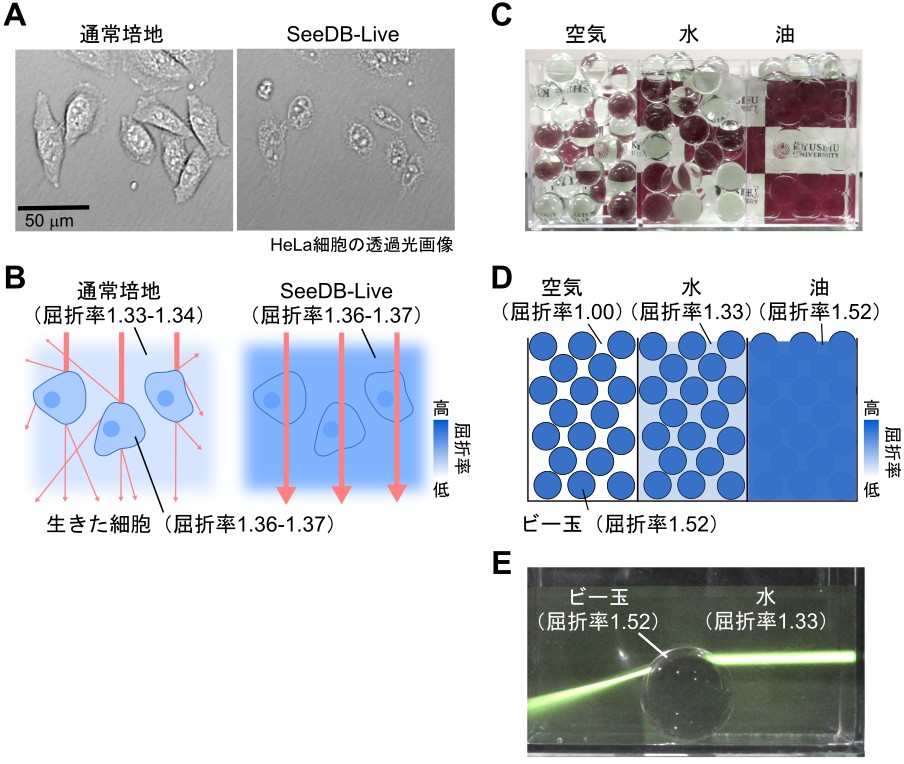
図2 細胞内外の屈折率を一致させることで生きた細胞が透明になる
(A) 細胞外液の屈折率を1.36-1.37にすることで、培養細胞が透明になる。SeeDB-Live では、アルブミンを通常培地に加えることで屈折率を調整している。
(B) 生きた細胞が透明になる仕組み。生きた細胞内部の屈折率は1.36-1.37と、通常培地の屈折率 (1.33-1.34) よりも高い。そのため、通常培地中では、細胞を透過する際に光が屈折・散乱し、組織中をまっすぐ進むことができない (左)。一方、細胞外液の屈折率を細胞内液と一致させると、光が直進するようになり、組織が透明になる (右、SeeDB-Live)。
(C) 細胞に見立てたビー玉 (屈折率1.52) を、空気 (屈折率1.0)、水 (屈折率1.33)、油 (屈折率1.52) に浸して観察した様子 (動画1)。
(D) ビー玉の見え方を説明した模式図。空気中や水中では、ビー玉の表面で光が屈折するため、後ろの市松模様は見えない (不透明)。一方、油中ではビー玉と屈折率が一致しているため、光がまっすぐ進み、後ろの市松模様がはっきり見える (透明)。
(E) 細胞に見立てたビー玉の表面でレーザーが屈折している様子。屈折率の異なる物質の境界で光は屈折する。同様に、細胞内の屈折率は通常培地よりも高いため、細胞を透過する際に光が屈折する。
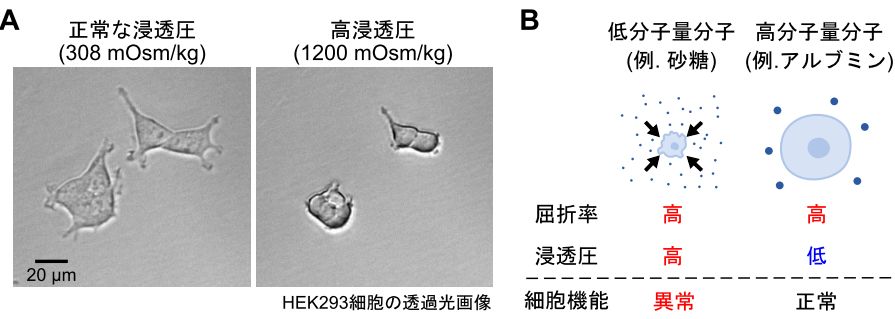
図3 浸透圧を上げずに屈折率を上げる方法
(A) 細胞外液の浸透圧が正常 (左、0.9%食塩水、浸透圧308 mOsm/kg) あるいは高い場合 (右、3.5%食塩水、浸透圧1200 mOsm/kg) の培養細胞 (HEK293 細胞) の形態。細胞外液の浸透圧が高いと、細胞内の水分が細胞外液に流出して収縮し、細胞の機能が損なわれてしまう。
(B) 屈折率を上げるために分子量の小さな分子 (低分子量分子) を溶かすと、単位体積当たりの分子数が著しく多くなるため、浸透圧が細胞内よりも高くなってしまう (左)。一方、分子量の大きな分子 (高分子量分子) の水溶液の場合、屈折率を上げるために必要な分子数は少なくて済むため、浸透圧の上昇は最小限に抑えられる (右)。そのため、ショ糖 (分子量342.3、濃度21.2%、1016 mOsm/kg) などを使うと細胞が収縮してしまうが、分子量の大きなアルブミン (分子量66,000、濃度18.7%、2.7 mOsm/kg) を用いて屈折率を調節しても、培地の浸透圧はほとんど上昇せず、細胞機能を正常に保つことができる。
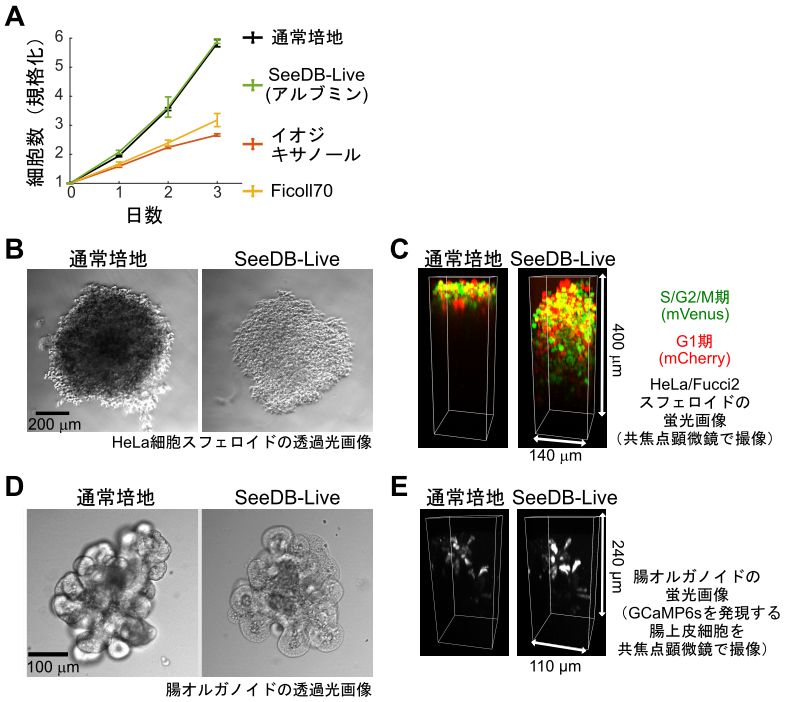
図4 生きた培養細胞スフェロイドおよび腸オルガノイドの透明化
(A) 培養細胞 (HeLa 細胞) の増殖実験。SeeDB-Live 中では、通常培地中と同程度の細胞増殖が確認された。イオジキサノールは X 線造影剤、Ficoll70 は球状のポリマーであり、どちらも高分子量分子であるが、細胞増殖は阻害された。
(B) 培養細胞スフェロイド (HeLa 細胞の細胞塊) の透過光画像 (動画2)。通常の培地中ではスフェロイドが不透明なため、黒い影が見えている。一方、スフェロイドを SeeDB-Live に浸すと、スフェロイドが透明になるため、光が透過するようになり、透明になった。
(C) 培養細胞スフェロイドの蛍光画像 (動画3)。SeeDB-Live により透明化され、蛍光タンパク質を発現する細胞を通常培地中と比べて2倍以上深くまで観察できるようになった。
(D) 腸オルガノイドの透過光画像。オルガノイドの表面では細胞が密に結合しているため、SeeDB-Live は組織内部にまでは浸透しないものの、オルガノイドの複雑な形状により生じる光の屈折が抑制され、オルガノイドが透明になった。
(E) 腸オルガノイドにおける細胞 (腸上皮細胞) の蛍光画像。SeeDB-Live により、蛍光カルシウムセンサー GCaMP6s からの蛍光を高いコントラストで検出できた。
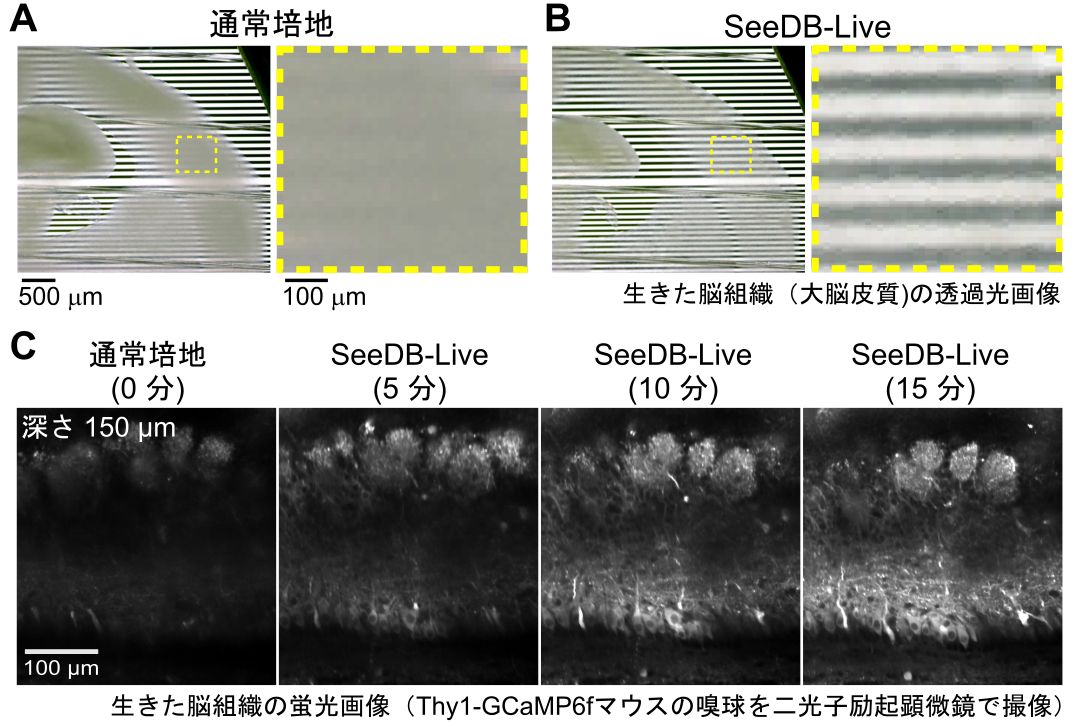
図5 生きた脳組織の透明化
(A, B) 生きた脳組織 (厚さ300マイクロメートルの切片) の透明化 (動画4)。通常培地 (人工脳脊髄液*10)、(A) および SeeDB-Live (B) に、それぞれ1時間ほど浸した後の生きた脳組織 (生後5日目マウスの大脳皮質) の透過光画像。透明化した脳組織では、標本の下に置いてあるしま模様が明瞭に観察できた。
(C) 生きた脳組織 (生後9日目マウスの嗅球) の蛍光カルシウム計測 (動画5)。神経細胞に蛍光カルシウムセンサー GCaMP6f を発現するトランスジェニックマウス Thy1-GCaMP6f の脳切片の蛍光を二光子励起顕微鏡で計測した。通常培地から SeeDB-Live に交換すると、脳組織が次第に透明化され、深部にある神経細胞の蛍光シグナルを計測できるようになった。
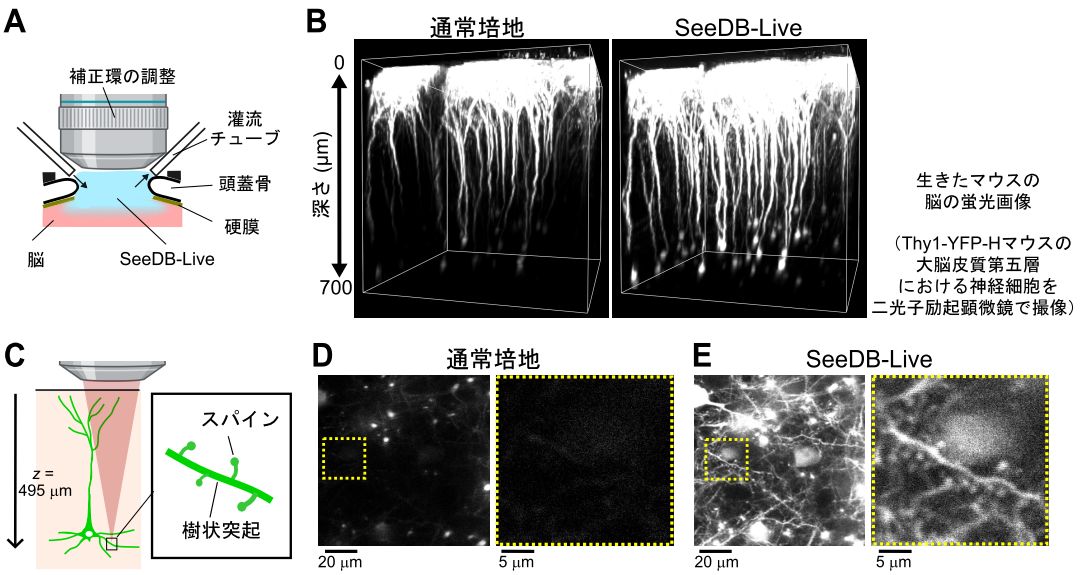
図6 生きた動物の脳の透明化
(A) 生きたマウスの脳の透明化。麻酔したマウスにおいて、脳表面に SeeDB-Live を1時間流し続けて浸透させ、透明化を行った。
(B) 大脳皮質第五層における神経細胞の三次元蛍光画像。蛍光タンパク質を神経細胞に発現する (Thy1-EYFP-H) マウスを二光子励起顕微鏡により撮像した。透明化前に比べ、透明化後では、脳深部における蛍光輝度が向上した (動画6、動画7)。
(C-E) 大脳皮質第五層における神経細胞の樹状突起や、樹状突起スパイン*11(C)。透明化前 (D) と比べ、透明化後 (E) には蛍光輝度が向上し、樹状突起や樹状突起スパインの蛍光画像がより明瞭に観察できるようになった。
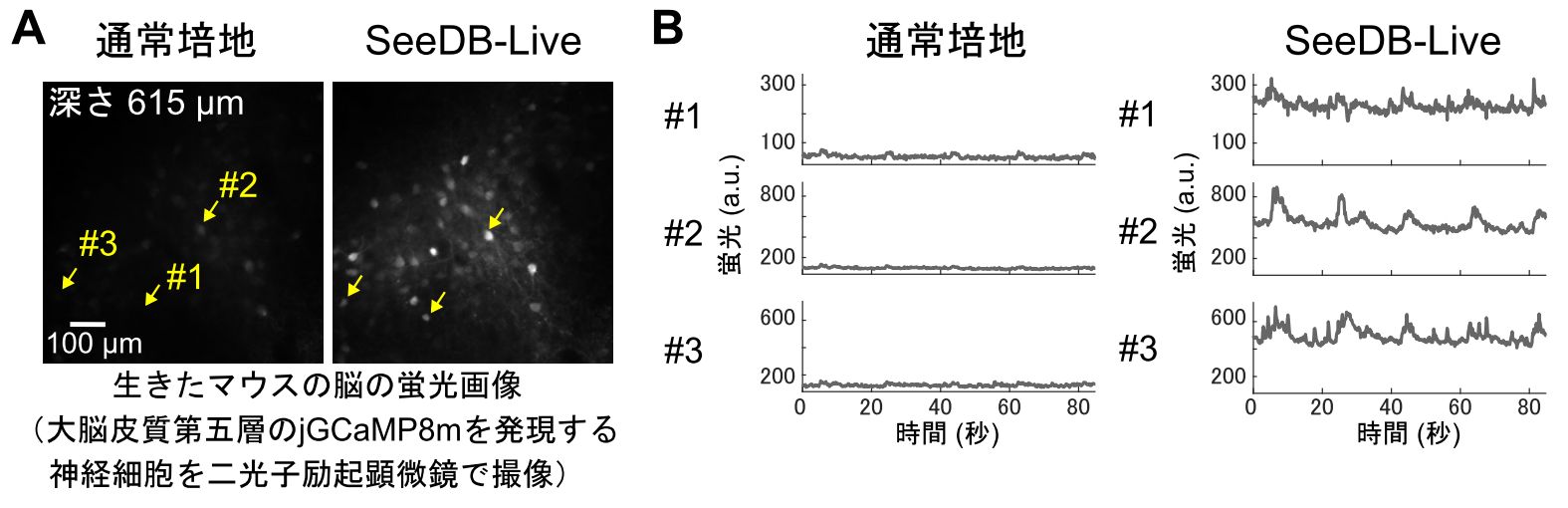
図7 生きた動物の脳深部におけるカルシウムシグナルの計測
(A) 大脳皮質 (第一次体性感覚野) 第五層における神経細胞の蛍光画像。SeeDB-Live によって、カルシウムセンサー jGCaMP8m からの蛍光シグナルを明瞭に観察できた。
(B) 透明化前後における神経細胞からの蛍光シグナルの経時変化。透明化前は、カルシウムセンサーの蛍光シグナルが暗く、その変化を十分に捉えることができない。一方、透明化後には、蛍光シグナルがより明瞭となり、その変化を捉えることができた。a.u., 任意単位 (相対値)
動画1 屈折率をそろえることでビー玉が透明になる様子
動画2 SeeDB-Live によるスフェロイドの透明化過程
動画3 スフェロイドが発現する蛍光タンパク質の観察
動画4 SeeDB-Live による生きた脳スライスの透明化過程
動画5 透明化に伴う脳スライス深部のカルシウムシグナルの向上
動画6 生きたマウスの脳の透明化過程 (蛍光タンパク質)
動画7 透明化前後における生きたマウス脳の蛍光観察
- *1 アルブミン
- アルブミンは肝臓で合成されるタンパク質であり、血漿 (血液のうち、血球成分を除いた液体成分のこと) 中に最も多く含まれる成分である。ヒト血漿中では一般的に4.4~5%の濃度で含まれており、水溶性が高い。ウシ血清由来アルブミン (BSA) が比較的安価で入手できることから、本研究では BSA を用いている。SeeDB-Live には BSA が約15% (質量濃度) 含まれている。
- *2 浸透圧
- 半透膜を隔てて水を移動させようとする力で、単位体積の溶液中に含まれる溶質分子やイオンの数に比例する。細胞を取り囲む細胞膜は半透膜 (水は通しやすいが溶質やイオンは通しにくい) としての性質があり、水は浸透圧の大きな方に移動する。細胞外液の浸透圧が細胞内よりも低すぎると細胞内に水が流入して破裂し、一方、高すぎると、細胞内から細胞外へと水が流出する。
- *3 屈折
- 物質の境界面で光の進む向きが変わる現象。光が屈折率の異なる物質の境界を斜めに通過するときに屈折が起こる。図2Eでは、水 (屈折率1.33) とガラス (屈折率1.52) の境界で光が屈折していることが分かる。異なる物質であっても、屈折率が同じであれば光はまっすぐに進む。
- *4 散乱
- 光が微小な粒子に当たることで、様々な方向に広がる現象。粒子 (散乱体) とその周囲の屈折率差が大きいほど散乱は強くなり、光はまっすぐ進みにくくなる。例えば、雲が白く見えるのは、微小な水滴 (屈折率1.33) と空気 (屈折率1.0) の間で屈折率が異なるためである。
- *5 蛍光センサー
- 特定の分子の濃度や活性を、蛍光の明るさや色の変化として可視化する分子。蛍光タンパク質や蛍光色素をもとに作られたものが多い。例えば、蛍光カルシウムセンサーは、細胞内のカルシウム濃度に応じて蛍光輝度が変化するため、生きた細胞の活動をリアルタイムに観察することができる。神経細胞においては、カルシウム濃度は発火 (活動電位、つまり神経細胞の電気的な活動のこと) の度合いを反映していることが知られている。
- *6 二光子励起顕微鏡
- 生体透過性の高い近赤外光のレーザーを用いて可視光域の蛍光観察を可能とする顕微鏡。通常の蛍光顕微鏡よりも組織の深い場所まで観察できるため、生きた組織や動物の蛍光観察に用いられる。
- *7 屈折率
- 光がどれだけ屈折するかを表す指標。物質中で光が進む速さに応じて値が変わる。水溶液の場合、溶質の種類や濃度によっても屈折率は異なる。真空や空気の屈折率は1.0、水の屈折率は1.33、油の屈折率は1.5程度である。例えば、糖を含む水溶液の場合、濃度が高くなるほど屈折率は高くなり、1.33から1.5程度まで変化する。
- *8 スフェロイド (細胞塊)
- 細胞が立体的に集まって形成される細胞集合体。単層の培養に比べて、細胞同士の相互作用や物質の拡散環境が生体に近く、実際の生体組織に近い性質を観察するのに適している。
- *9 オルガノイド
- 生体組織や ES 細胞などの多能性幹細胞から作られる、臓器の形や機能を部分的に再現した三次元組織。ミニ臓器とも呼ばれ、薬の開発や再生医療、組織形成の研究などに用いられる。
- *10 人工脳脊髄液
- 脳脊髄液 (脳の細胞外液) のイオン組成を人工的に模倣した溶液。神経細胞や脳組織を生きた状態で保つために実験で広く用いられる。
- *11 樹状突起、樹状突起スパイン
- 神経細胞から伸びる突起構造のうち、主に入力に特化したものを樹状突起という。その表面に多数存在する小突起を樹状突起スパイン (もしくは棘突起 (きょくとっき))と呼ぶ。樹状突起スパインは、他の神経細胞の軸索 (出力に特化した突起構造) と接触してシナプスと呼ばれる構造をつくり、入力信号を受け取る場として機能する。
本研究は、科学技術振興機構 (JST) 戦略的創造研究推進事業 CREST 研究領域「多細胞間での時空間的相互作用の理解を目指した定量的解析基盤の創出」研究課題名「腸-脳機能コネクトミクスによる腸内感覚の機能解明と操作」(JPMJCR2021)、JST 創発的研究支援事業 (JPMJFR230P)、日本医療研究開発機構 (AMED) (JP23wm0525012, JP25wm0625128, JP19dm0207080, JP19dm0207079, JP23gm6510022, JP24wm0625119)、文部科学省・日本学術振興会 (JSPS) 科研費 学術変革領域 (A)「動的コネクトームに基づく脳機能創発機構の解明」(JP24H02308, JP24H02312)、JSPS 科学研究費助成事業 (JP19K06886, JP20K23378, JP21H00205, JP21H02140, JP21H05696, JP22H00460, JP22H02718, JP22H05094, JP22H05161, JP22K06446, JP22K18373, JP23H02577, JP23H04236, JP23K06151, JP23K18161, JP23K18165, JP24H00861, JP24H01289, JP24K01702, JP24K02132, JP24K18240, JP25H02500, JP25K02560, JP25KJ1906)、鹿児島大学めぐみ会医学研究推進基金、世界トップレベル研究拠点プログラム (WPI-PRIMe)、持田記念医学薬学振興財団、および上原記念生命科学財団の助成を受けました。
- 掲載誌:
- Nature Methods
- タイトル:
- Isotonic and minimally invasive optical clearing media for live cell imaging ex vivo and in vivo
- 著者名:
- Shigenori Inagaki, Nao Nakagawa-Tamagawa, Nathan Zechen Huynh, Yuki Kambe, Rei Yagasaki, Satoshi Manita, Satoshi Fujimoto, Takahiro Noda, Misato Mori, Aki Teranishi, Hikari Takeshima, Koki Ishikawa, Yuki Naitou, Tatsushi Yokoyama, Masayuki Sakamoto, Katsuhiko Hayashi, Kazuo Kitamura, Yoshiaki Tagawa, Satoru Okuda, Tatsuo K. Sato, Takeshi Imai
(稲垣成矩、玉川 (中川) 直、フイン・ネイサン、神戸悠輝、矢ケ崎怜、真仁田聡、藤本聡志、野田貴大、森美咲都、寺西亜生、武島光里、石河幸樹、内藤優希、横山達士、坂本雅行、林克彦、喜多村和郎、田川義晃、奥田覚、佐藤達雄、今井猛) - DOI:
- 10.1038/s41592-026-03023-y
九州大学 大学院医学研究院 疾患情報研究分野
教授 今井 猛(イマイ タケシ)
TEL:092-642-6090 E-Mail:imai.takeshi.457(at)m.kyushu-u.ac.jp
- 2026年3月13日付の日刊工業新聞に掲載されました。
- 2026年3月13日付の西日本新聞に掲載されました。

